02/10/2023
A história dos cientistas premiados pela tecnologia que levou às vacinas de Pfizer e Moderna
Hungara Katalin Karikó e americano Drew Weissman foram reconhecidos pelas descobertas relacionadas às modificações nas bases nucleotídicas que permitiram o desenvolvimento das vacinas de mRNA contra a covid-19
O Prêmio Nobel de Medicina
e Fisiologia de 2023 foi dado aos cientistas Katalin Karikó e Drew Weissman.
Karikó nasceu na Hungria em
1955 e se especializou em bioquímica. Ela trabalha na farmacêutica BioNTech e é professora da Universidade
da Pensilvânia, nos Estados Unidos.
 Cientistas premiados com o Nobel de Medicina 2023. (Foto: BBC)
Cientistas premiados com o Nobel de Medicina 2023. (Foto: BBC)Mini-impressoras dentro de
nós
Com exceção de óvulos
e espermatozoides, todas as células do nosso corpo carregam dentro do núcleo o genoma completo, o DNA.
Nesse conjunto de cromossomos, estão
"escritas" muitas das informações que definem os processos orgânicos, as características físicas
e a propensão a determinadas doenças de cada um de nós.
Mas o DNA sozinho não faz
nada: quando ele precisa enviar algum comando à célula, essa fita em dupla hélice gera uma cópia
simples de determinado trecho do código genético.
Esse "xerox" genético vem
numa fita simples e é o que conhecemos como RNA mensageiro, ou mRNA.
Esse material então sai do
núcleo e viaja até os ribossomos, no citoplasma da célula. Essa estrutura lê a "receita" genética
do mRNA e fabrica uma proteína específica relacionada àquele comando escrito no DNA.
Desde que esse mecanismo foi conhecido,
a partir dos anos 1960, os cientistas começaram a se perguntar: será que é possível aproveitar
essas "mini-impressoras" que carregamos dentro das células para produzir proteínas específicas?
O objetivo era que essas proteínas
tivessem algum fim terapêutico, e pudessem servir para gerar uma resposta do sistema imunológico — o que
permitiria combater o crescimento de um tumor ou a invasão de um vírus mortal, por exemplo.
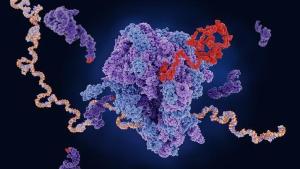 O mRNA (fita amarela e azul) viaja até o ribossomo (roxo
e azul, no centro da imagem), que produz uma proteína (vermelho). (Foto: BBC)
O mRNA (fita amarela e azul) viaja até o ribossomo (roxo
e azul, no centro da imagem), que produz uma proteína (vermelho). (Foto: BBC)Pedras pelo caminho
Mas é claro que a ideia não
funcionou logo de cara. A principal barreira a ser superada tinha a ver com o fato de o mRNA ser uma molécula muito
frágil — como se trata apenas de uma mensageira, ela logo se degrada no organismo.
Nos primeiros experimentos, os mRNAs
sintetizados em laboratório sequer conseguiam chegar perto das células. Eles estragavam pelo caminho, antes
de cumprir a missão para o qual foram projetados.
Além disso, esses compostos
se mostraram altamente inflamatórios. Eles geraram uma reação imunológica forte, que colocava
em risco o próprio uso desse princípio na medicina.
Essas dificuldades foram superadas
graças a dois trabalhos distintos. O primeiro deles, comandado pelo justamente médico americano Drew Weissman
e pela bioquímica húngara Katalin Karikó, descobriu que algumas modificações básicas
na estrutura do mRNA poderiam deixá-lo menos inflamatório.
Esse esforço, aliás,
rendeu à dupla o Prêmio Nobel de Medicina e Fisiologia de 2023.
O segundo, que envolveu vários
grupos de pesquisa, como o comandado pelo bioquímico canadense Pieter Cullis, descobriu que "embrulhar" a fita de mRNA
numa nanopartícula de lipídios (ou gordura) é uma forma eficaz de protegê-lo da degradação.
Assim, essa molécula pode ser injetada, viajar pelo organismo e chegar às células onde cumprirá
a função para a qual foi projetada.
"Com essas modificações,
a ciência estava diante de uma ferramenta potente e poderosa", disse o biomédico Joel Rurik, da Universidade
da Pensilvânia, nos Estados Unidos, numa entrevista à BBC News Brasil em maio de 2023.
"Trabalhar com o mRNA é algo
relativamente simples e rápido. Basta fazer o download da sequência genética no computador e pedir para
uma bioimpressora imprimir este material. Você consegue produzir toneladas dele sem a necessidade de usar uma única
célula", complementou o cientista.
"Falamos, portanto, de uma estratégia
eficaz do ponto de vista dos custos, estável, com facilidade de distribuição e que pode ser usada de
forma mais ampla ou fácil que muitas ferramentas terapêuticas ou de engenharia imunológica", resumiu.
 Pesquisas que levaram à premiação. (Foto: BBC)
Pesquisas que levaram à premiação. (Foto: BBC)'Estreia' antecipada
Ainda que os testes clínicos
com as primeiras vacinas de mRNA tenham começado no início dos anos 2000, a comunidade científica esperava
que as primeiras versões comercialmente disponíveis, aprovadas pelas agências regulatórias, só
chegassem ao mercado em meados de 2025.
Até que veio a covid-19 e
tudo mudou. A emergência da pior pandemia em um século exigiu que muitos especialistas mudassem os planos e começassem
a estudar um vírus absolutamente novo: o Sars-CoV-2.
Assim que o sequenciamento genético
do causador da covid foi concluído, ainda em janeiro de 2020, os grupos que já trabalhavam com imunizantes de
mRNA para outros patógenos (como o vírus sincicial respiratório) direcionaram os esforços para
o novo coronavírus.
Em março daquele mesmo ano,
os primeiros estudos clínicos dessas vacinas começaram a acontecer. Dez meses depois, em dezembro, a Food and
Drug Administration (FDA), a agência regulatória dos EUA, aprovou os dois produtos com a tecnologia mRNA desenvolvidos
e testados pelas farmacêuticas Moderna e Pfizer/BioNTech.
Pouco depois, eles também
foram liberados em outras partes do mundo — no Brasil, a Agência Nacional de Vigilância Sanitária
(Anvisa) deu sinal verde para o uso do imunizante da Pfizer em 23 de fevereiro de 2021.
Essa foi a primeira vez na história
que uma vacina de mRNA — baseada nos trabalhos pioneiros de Karikó e Weissman — chegou ao braço
das pessoas fora do ambiente das pesquisas científicas.
Ela se baseia naquele princípio
explicado no início desta reportagem: cada dose do produto traz uma fita de RNA mensageiro (mRNA), que instrui as células
do nosso próprio organismo a fabricar a proteína S (de Spike, ou espícula em português) presente
na superfície do coronavírus.
A partir daí, o sistema imunológico
reconhece esse material e gera uma resposta, capaz de proteger caso o agente infeccioso de verdade tente invadir o corpo.
O que vem por aí
Logo após a experiência
com a covid-19, o próximo "passo natural" para o mRNA é que ele seja usado para desenvolver vacinas contra outras
doenças infecciosas.
Inclusive, laboratórios já
estão realizando testes de imunizantes contra todos os tipos de coronavírus, o influenza, o zika, o chikungunya,
a dengue, a malária, o HIV, entre outros.
Segundo o ClinicalTrials.Gov, site
que registra todos os testes clínicos em andamento nos Estados Unidos, existem cerca de 800 estudos do tipo em andamento
que avaliam algum aspecto dessa plataforma tecnológica.
Rurik classificou esse campo da ciência
como "empolgante".
"As vacinas de mRNA usadas contra
a covid-19 lançaram um enorme holofote na área. Com isso, vieram os investimentos privados e os programas governamentais
de incentivo", contextualizou.
O próprio trabalho do biomédico
é um exemplo disso. Nos últimos anos, ele investiga se o mRNA pode servir como uma ferramenta para que as células
de defesa reconheçam e destruam fibroblastos "doentes" no coração.
Os fibroblastos são um tipo
de célula que forma a estrutura do músculo cardíaco. Quando essas unidades apresentam algum tipo de defeito,
isso pode representar a origem de uma doença crônica (como a insuficiência cardíaca) ou aguda (como
o infarto).
"Treinar" as células imunológicas
para identificar os fibroblastos defeituosos, portanto, pode se tornar, no futuro, um caminho para prevenir as condições
que afetam o coração.
Ainda no mundo da cardiologia, outros
grupos trabalham com o mRNA como uma forma de baixar o LDL, o colesterol ruim. Essa molécula está diretamente
relacionada com uma série de desfechos perigosos, como o próprio infarto e o Acidente Vascular Cerebral (AVC).
Isso porque algumas pessoas possuem
um gene que faz elas expressarem demais uma proteína chamada PCSK9, o que leva o colesterol às alturas. Inibir
essa fabricação excessiva por meio do mRNA poderia ser um caminho para lidar de forma definitiva com esse fator
de risco para tantas doenças cardiovasculares.
Aos poucos, a tecnologia do mRNA
também volta às suas origens: as pesquisas sobre o uso dessas vacinas contra tumores começaram a ganhar
mais fôlego nos últimos meses.
Afinal, o câncer é uma
fonte de muitas mutações genéticas. Além disso, ele tem a característica de produzir certas
moléculas capazes de suprimir o sistema imunológico.
Em outras palavras, as células
cancerosas são capazes de produzir determinadas substâncias que bloqueiam a imunidade. Com isso, as unidades
de defesa não reconhecem a ameaça — e o tumor cresce no corpo sem encontrar resistência.
Já existem atualmente tratamentos
que tiram essa "venda" das unidades de defesa e permitem que o próprio sistema imunológico passe a atacar o
câncer. Esse grupo de fármacos é conhecido como imunoterapia, e está disponível contra o
melanoma e outros tipos da doença.
Mas e se fosse possível aplicar
uma vacina de mRNA para que o organismo do paciente identificasse certas mutações tumorais mais comuns? Ou ainda
criar um produto farmacêutico totalmente personalizado, baseado nas alterações genéticas que aparecem
em cada indivíduo com câncer?
Além disso, um dos grandes
sonhos da oncologia sempre foi desenvolver uma espécie de ‘memória imunológica’ contra o
câncer, de modo que o sistema imune saiba quando o tumor retornou ou está se espalhando para outros tecidos.
Todas essas possibilidades estão
sendo testadas agora por grupos de pesquisas e farmacêuticas.
O passo concreto mais recente do
mRNA contra o câncer foi anunciado pelos laboratórios Moderna e MSD em abril: uma vacina experimental contra
o melanoma foi capaz de diminuir o risco de morte em 44% quando associado à imunoterapia.
Vale ponderar, no entanto, que o
produto ainda está em desenvolvimento e precisa passar por novas etapas de estudo antes de chegar às clínicas
e aos hospitais.
Por fim, Rurik apontou que o mRNA
não é mais uma plataforma exclusiva para doenças infecciosas, cardíacas ou oncológicas.
"Também já vemos estudos
em andamento para tratar lúpus e outras doenças autoimunes", exemplifica.
Mas, para que isso realmente aconteça,
os cientistas precisarão ainda trabalhar bastante para provar a segurança e a eficácia de tantas novidades.
O principal desafio será demonstrar
que todas essas terapias não geram problemas no sistema imunológico ou prejudicam o funcionamento de órgãos
vitais, como o fígado.
"Mas é inegável que
há muita coisa acontecendo agora com o mRNA, e tenho certeza que ideias ‘malucas’, que imaginávamos
impossíveis, virarão realidade nos próximos cinco anos", concluiu o biomédico.
Fonte: BBC


